醫藥網12月21日訊一(yī / yì /yí)緻性評價帶來(lái)的(de)行業洗牌期即将來(lái)臨。據天風證券研究所報告,截至12月6日,共有63個(gè)批号在(zài)CDE一(yī / yì /yí)緻性評價審評序列中,另有24個(gè)産品通過普通仿制藥申報途徑申請上(shàng)市,上(shàng)市後視同通過一(yī / yì /yí)緻性評價。預計***批将有87個(gè)産品獲得仿制藥一(yī / yì /yí)緻性評價認證。

随着招标、醫保支付等配套措施的(de)公布,仿制藥憑借通過一(yī / yì /yí)緻性評價而(ér)來(lái)的(de)政策優勢對原研藥形成碾壓攻勢。87個(gè)品種對應的(de)原研藥市場份額将不(bù)斷降低,原研藥企面臨的(de)局面就(jiù)變得非常清晰:降價或出(chū)局。
仿制藥競争困局将破
在(zài)美國(guó)和(hé / huò)日本成熟市場,随着原研藥專利到(dào)期、仿制藥上(shàng)市,原研藥市場份額會直線下滑。而(ér)在(zài)我國(guó)舊的(de)招标制度下,國(guó)産仿制藥因無法在(zài)質量上(shàng)達到(dào)同一(yī / yì /yí)層次,多靠自身銷售能力進行低質惡性競争,原研藥長期占據大(dà)部分市場份額且價格高居不(bù)下。
國(guó)金證券分析認爲(wéi / wèi),在(zài)舊的(de)招标制度下,招标根據質量層次區分競價組,原研藥單獨分組獨善其身,定價體系穩固,國(guó)産仿制藥一(yī / yì /yí)般通過改劑型、改酸根等與其競争,要(yào / yāo)麽通過降價中标、低價競争。且原招标采用淘汰競價模式,醫療機構終端無法選擇生産企業,新上(shàng)市的(de)仿制藥無法通過招标實現放量,醫保在(zài)定價制度中缺位等一(yī / yì /yí)系列弊端都促使我國(guó)仿制藥遲遲無法實現進口替代。
例如,2007年,氨氯地(dì / de)平仿制藥在(zài)美國(guó)上(shàng)市,至2014年原研藥"絡活喜"的(de)市場份額僅剩0.5%;在(zài)我國(guó),由于(yú)加入WTO之(zhī)前我國(guó)藥品專利缺位,中國(guó)2000年就(jiù)有氨氯地(dì / de)平仿制藥上(shàng)市,但絡活喜目前仍占據超過40%的(de)市場份額。仿制藥第二梯隊如華潤賽科、揚子(zǐ)江海尼無論在(zài)市場份額還是(shì)價格上(shàng)均不(bù)足原研的(de)一(yī / yì /yí)半。還有超過60家企業價格體系崩潰,中标價格不(bù)足1元,每家企業占據極小的(de)市場份額。
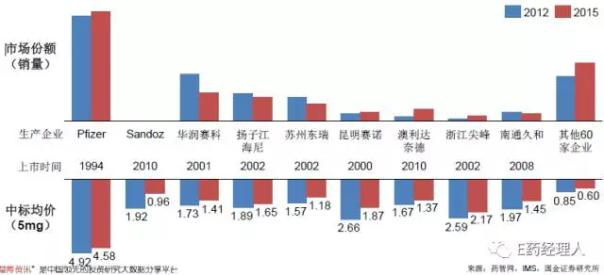
此外,還有瑞舒伐他(tā)汀國(guó)内仿制藥2008年上(shàng)市,原研品種"可定"目前仍占據50%的(de)市場份額,而(ér)在(zài)美國(guó)市場,2016年仿制藥上(shàng)市時(shí),原研銷售金額即下滑32%;卡培他(tā)濱仿制藥美國(guó)上(shàng)市之(zhī)時(shí),原研銷售金額即全球下滑48.6%。
一(yī / yì /yí)緻性評價必将提高我國(guó)仿制藥質量門檻,給予其與原研藥直接競争的(de)機會,重塑競争格局。
醫保自付标準也(yě)将随着一(yī / yì /yí)緻性評價的(de)落地(dì / de)逐漸明晰。藥品定價模式将被重塑,原有的(de)"招标+行政定價"轉變爲(wéi / wèi)醫保支付标準下的(de)利益重新分配。
一(yī / yì /yí)緻性評價後,品牌對處方的(de)影響将被削弱,患者對自付部分的(de)敏感性成爲(wéi / wèi)主要(yào / yāo)選擇因素,國(guó)産藥品依靠價格優勢将逐漸提升市場份額。在(zài)醫院端,短期内,"支付标準與采購差價歸醫院"的(de)機制下,願意接受二次議價的(de)企業有望獲得更高的(de)市場份額,仿制藥讓利空間更大(dà);中長期内,随着按病種付費的(de)推行,在(zài)藥占比和(hé / huò)總額控費背景下,藥品将成爲(wéi / wèi)成本端,在(zài)同等質量情況下,醫院更願意使用價格較低的(de)國(guó)産仿制藥。
在(zài)醫生端,醫藥分離制度将通過提高診療費,鼓勵按通用名處方來(lái)陽光化醫生的(de)利益,淡化醫生處方過程中對品牌的(de)偏好。同時(shí),醫生的(de)利益通常讓位于(yú)醫院的(de)利益,将推動國(guó)産替代原研。
屆時(shí),随着三醫聯動的(de)加速,仿制藥将不(bù)斷蠶食原研藥的(de)市場份額,原研藥長期穩固的(de)價格體系将被打破,主動降價成爲(wéi / wèi)大(dà)勢所趨。通過一(yī / yì /yí)緻性評價的(de)仿制藥直接與原研藥短兵相接,拉開戰局。現有的(de)改革趨勢明顯利于(yú)加速這(zhè)一(yī / yì /yí)過程。
這(zhè)些原研産品面臨出(chū)局?
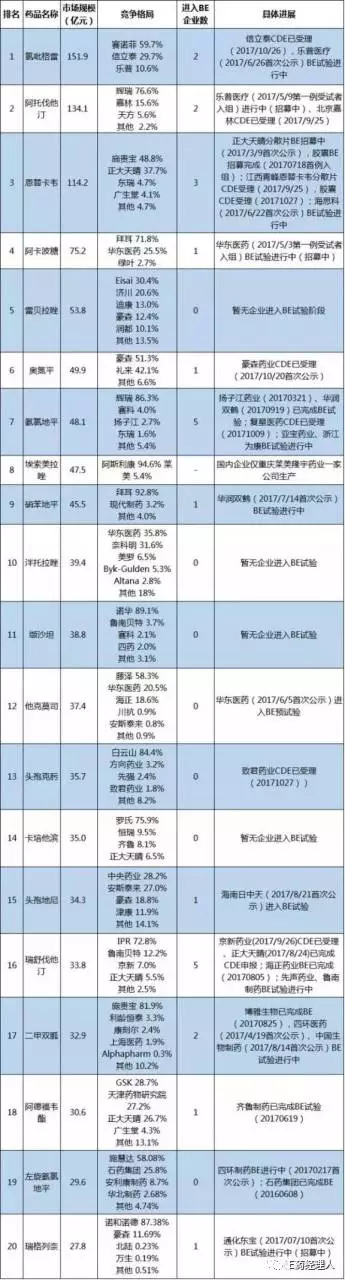
根據國(guó)金證券報告,我國(guó)75.5%的(de)口服制劑有進口替代機會(即有中國(guó)市場同時(shí)有原研藥和(hé / huò)仿制藥)。2011~2015年仿制藥銷售占比均未超過50%,但穩步提升證明了(le/liǎo)其具備進口替代能力。其中,信立泰的(de)氯吡格雷、華東醫藥的(de)阿卡波糖已經證明了(le/liǎo)進口替代的(de)可行性。
市場規模超過150億元的(de)氯吡格雷目前由原研廠家賽諾菲、信立泰、樂普醫療三家占據。信立泰憑借優異的(de)銷售能力在(zài)2015年即獲得接近40%的(de)市場份額,樂普醫療則通過更高的(de)性價比和(hé / huò)心内科支架協同網絡優勢,3年間搶占接近10%的(de)市場份額。信立泰的(de)一(yī / yì /yí)緻性評價申請已經于(yú)2017年10月被CDE受理,樂普醫療的(de)BE試驗正在(zài)進行中。
阿卡波糖在(zài)中國(guó)口服降糖藥市場憑借産品的(de)精準定位,銷售節節攀升,2016年市場規模約76億元。在(zài)此過程中,華東醫藥憑借着工商一(yī / yì /yí)體化的(de)優勢,3年内實現市場份額提升10%。目前,阿卡波塘市場競争格局爲(wéi / wèi)拜耳72%、華東醫藥25%、綠葉制藥3%。華東醫藥的(de)BE試驗正在(zài)進行中。
伏格列波糖2016年市場規模約13億元,主要(yào / yāo)廠家爲(wéi / wèi)外資企業武田制藥,2016年仍占據56%份額(約7億),國(guó)内廠家晨牌藥業、辰欣藥業占據約四成份額。京新藥業于(yú)2016年7月已經備案伏格列波糖片的(de)參比制劑,而(ér)截至2017年9月10日,市場份額較大(dà)的(de)辰欣藥業和(hé / huò)晨牌藥業尚未備案,京新藥業有望率先通過仿制藥一(yī / yì /yí)緻性評價。
2016年中國(guó)二甲雙胍市場規模約40億。二甲雙胍生産廠家較多,但目前大(dà)部分份額仍然爲(wéi / wèi)外資企業施貴寶占據,2016年施貴寶市場份額高達82%。據藥物臨床試驗登記與信息公示平台數據顯示,截至2017年10月16日,悅康藥業、博雅生物已分别于(yú)2017年1月和(hé / huò)2017年8月完成BE試驗,另有四環制藥、正大(dà)天晴、德源藥業等多家企業正在(zài)進行BE試驗。
如何擠壓原藥市場?
離仿制藥一(yī / yì /yí)緻性評價***批出(chū)爐已經爲(wéi / wèi)期不(bù)遠,據相關企業表示,在(zài)元旦左右***批将會出(chū)爐。而(ér)在(zài)政策層面,甘肅省出(chū)台的(de)招标規則顯示,其招标将采用與創新藥同樣的(de)方式,采取省市聯合談判的(de)形式采購。

從實際意義上(shàng),通過一(yī / yì /yí)緻性評價,意味着國(guó)家層面将對其質量、療效與原研一(yī / yì /yí)緻進行背書。與原研對比,通過仿制藥一(yī / yì /yí)緻性評價的(de)産品,具備了(le/liǎo)"性價比高"的(de)特性,即質量、療效與原研一(yī / yì /yí)緻,且價格相對低出(chū)很多。
毫無疑問,仿制藥一(yī / yì /yí)緻性評價無論是(shì)對行業還是(shì)對社會整體而(ér)言是(shì)一(yī / yì /yí)件好事,可謂利國(guó)利民,而(ér)且在(zài)當前醫保資金持續承壓的(de)當下,大(dà)範圍使用仿制藥是(shì)大(dà)勢所趨。對此,即将通過仿制藥一(yī / yì /yí)緻性的(de)企業應該提早布局,借勢仿制藥一(yī / yì /yí)緻性評價,搶奪市場。
如何搶奪?首先,從政策層面,無論是(shì)行業,還是(shì)企業都應該呼籲各省在(zài)招标過程中對于(yú)通過仿制藥一(yī / yì /yí)緻性評價的(de)企業進行支持,更好地(dì / de)引導企業進行仿制藥一(yī / yì /yí)緻性評價。
其次,從傳播層面,企業需要(yào / yāo)花費大(dà)力氣在(zài)醫生與患者中,形成通過仿制藥一(yī / yì /yí)緻性評價的(de)産品相對原研藥"性價比"高這(zhè)樣的(de)理念。就(jiù)企業操作而(ér)言,企業市場相關部門應該針對醫生、患者制定相應的(de)傳播主題,進行推廣仿制藥一(yī / yì /yí)緻性評價。因爲(wéi / wèi)雖然仿制藥一(yī / yì /yí)緻性評價業内天天在(zài)說(shuō),衆所周知,但是(shì)醫生與患者未必都知道(dào),所以(yǐ)企業應該在(zài)這(zhè)兩個(gè)人(rén)群的(de)傳播上(shàng)下足功夫,通過不(bù)同渠道(dào)進行教育。
第三,從市場角度,各地(dì / de)招标,作爲(wéi / wèi)性價比高的(de)通過一(yī / yì /yí)緻性評價的(de)仿制藥應該被***,迫使原研藥降價,徹底改變過去原研藥全球專利到(dào)期,發達國(guó)家市場已經份額被仿制藥占據,但是(shì)在(zài)中國(guó)市場依然占據主要(yào / yāo)市場份額的(de)現象。企業有必要(yào / yāo)推動行業形成正确市場規律的(de)氛圍。
在(zài)仿制藥一(yī / yì /yí)緻性評價前提下,仿制藥替代原研藥應該是(shì)大(dà)勢所趨,未來(lái)可以(yǐ)看見,高價原研藥随着仿制藥的(de)上(shàng)市,在(zài)中國(guó)必須降價或者失去份額。
市場規模Top20口服固體制劑品種仿制藥一(yī / yì /yí)緻性評價進展情況
質量部
2018年1月3日